贡献者: addis
我们来从微观的角度考察气体是如何对一个光滑平面产生压强的。一种错误的解释是:每个气体分子像一个有弹性的小球,他们互紧挨着,对彼此和容器壁产生压力,当体积越小,压力也就越大。然而真实情况1是,气体分子之间的距离远远大于他们的体积,且都在不断运动。是大量分子撞击容器壁产生的 “冲击力” 对容器产生了等效的压力。这种撞击可以看作是在一瞬间完成的,就像高中学的完全弹性碰撞。所以我们需要使用动量和冲量。
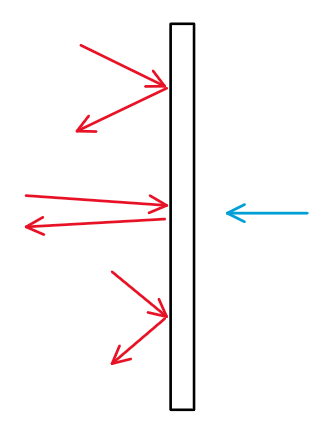
图 1:分子对容器壁的压强
如图 1 ,我们假设空间中没有重力,向右为 $x$ 方向,一块面积为 $S$ 的光滑平板初始时静止,令其质量为 $M$,远大于分子的质量。平板的左侧不断受到大量粒子从各个随机方向,以各种随机速度的撞击。虽然每个分子的动量很小,但撞击的频率却很大(数量级与阿伏伽德罗常数相当,即 $10^{24}$ 次每秒)。由于这些撞击的位置完全是随机的,他们可以被等效为一个均匀的压强。如何定义等效压强呢?我们可以在平板的右侧对平板施加一个均匀恒定的 “真正的” 压强 $P$(或者等效地,直接施加恒力 $F = PS$),如果左边分子的撞击和右边的压强能使平板保持宏观的静止,那么我们就说分子撞击对平板的(等效)压强为 $P$。
我们给这些分子编号,假设第 $i$ 个分子延 $x$ 方向的速度分量为 $v_{x,i}$,质量都为 $m$,则碰撞前延 $x$ 方向的动量为 $p_i = m v_{x,i}$。由于平板的质量远大于单个分子的质量,撞击以后可以认为分子 $x$ 方向的速度取相反数,而平行于平板方向的速度不变(类似于光的镜面反射)。这样,碰撞后单个分子的动量变化(即冲量)为 $\Delta p_i = -2mv_{x,i}$,由动量守恒,平板的动量瞬间增加了 $2mv_{x,i}$。如果一段时间 $\Delta t$ 内,有 $N$ 个分子撞击平板,则平板受到向右的总冲量为
\begin{equation}
\Delta p = \sum_{i=1}^N 2mv_{x,i} = 2m \sum_{i=1}^N v_{x,i}~,
\end{equation}
再来看右边的压力对平板的作用。$\Delta t$ 时间内该作用力对平板向左的冲量为
\begin{equation}
\Delta p = PS \Delta t~.
\end{equation}
若要使平板在宏观上不动,总冲量必须为零,以上两式相等,即
\begin{equation}
P = \frac{2m}{S\Delta t} \sum_{i=1}^N v_{x,i} = 2m\bar v_{x,i} \frac{N}{S\Delta t}~.
\end{equation}
其中我们定义 $x$ 方向速度平均值为
\begin{equation}
\bar v_{x,i} = \frac{1}{N}\sum_{i=1}^N v_{x,i}~.
\end{equation}
也就是说,等效压强和分子在垂直容器壁方向的平均动量成正比,与单位面积单位时间撞击容器壁的粒子数成正比。
1. 两块平板
我们再来讨论一个稍微复杂一些的情况。假设空间中有两块平行平板,他们之间距离为 $a$,每个粒子会在这两块平板之间来回反弹(假设不飞出边界),第 $i$ 个粒子来回运动一次的周期是 $T_i = 2a/v_{x,i}$,$\Delta t$ 时间(假设远大于 $T_i$)内可以与右边的平板发生碰撞的次数为
\begin{equation}
N_i = \frac{\Delta t}{T_i} = \frac{v_{x,i} \Delta t}{2a}~,
\end{equation}
所有的分子在 $\Delta t$ 时间内碰撞右壁的次数为 $N = \sum N_i$。
所以 $\Delta t$ 时间内,右侧平板获得的总冲量为
\begin{equation}
\Delta p = \sum_{i=1}^N 2mv_{x,i} N_i = \frac{m \Delta t}{a} \sum_{i=1}^N v_{x,i}^2 = m\overline {v_{x,i}^2} \frac{ N\Delta t}{a}~,
\end{equation}
其中我们定义了速度平方得平均值(注意这与
式 4 的平方 $\bar v_{x,i}^2$ 不同)
\begin{equation}
\overline {v_{x,i}^2} = \frac{1}{N} \sum_{i=1}^N v_{x,i}^2~.
\end{equation}
与上面同理,为了保持总冲量相等,
式 6 和
式 2 必须相等,得
\begin{equation}
P = m \overline {v_{x,i}^2} \frac{N}{Sa}~.
\end{equation}
从这个公式出发,我们很容易可以得到理想气体状态方程。注意这里的 $Sa$ 就是两平板之间的体积,而 $mv_{x,i}^2$ 就是单个分子动能 $E_{k,i}$ 的两倍。
1. ^ 除了极端温度或压强的情况
致读者: 小时百科一直以来坚持所有内容免费无广告,这导致我们处于严重的亏损状态。 长此以往很可能会最终导致我们不得不选择大量广告以及内容付费等。 因此,我们请求广大读者
热心打赏 ,使网站得以健康发展。 如果看到这条信息的每位读者能慷慨打赏 20 元,我们一周就能脱离亏损, 并在接下来的一年里向所有读者继续免费提供优质内容。 但遗憾的是只有不到 1% 的读者愿意捐款, 他们的付出帮助了 99% 的读者免费获取知识, 我们在此表示感谢。