囊胚
编辑囊胚是哺乳动物早期发育形成的一种结构。它拥有一个内细胞团(ICM),随后形成胚胎。囊胚的外层由统称为滋养层的细胞组成。这层包围着内细胞团和一个被称为囊胚腔的充满液体的腔。滋养层产生胎盘。“囊胚”这个名字来自希腊语βλαστόςblastos (“芽”)和κύστις kystis (“囊状物,胶囊”)。
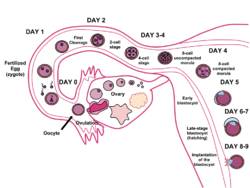
在人类中,囊胚在受精后大约5天开始形成,此时桑椹胚(一个细胞球)中出现一个充满液体的腔。囊胚直径约为0.1-0.2毫米,在快速卵裂(细胞分裂)后包含200-300个细胞。囊胚形成后约1天(受精后5-6天),也就是囊胚通常到达子宫的时候,囊胚开始嵌入子宫壁的子宫内膜中,在那里它将经历进一步的发育过程,包括原肠胚形成。囊胚嵌入子宫内膜需要从透明带孵化出来,当前胚胎进入子宫时,透明带会阻止其粘连在输卵管上。受精后仅11-12天囊胚就完全嵌入子宫内膜。
囊胚在体外受精(IVF)中的应用包括在将受精卵植入子宫前培养五天。这可能是一种比传统试管受精更可行的生育治疗方法。囊胚的内细胞团是胚胎干细胞的来源。
1 发育周期编辑
在人类胚胎形成过程中,受精后大约5-6天,桑椹胚细胞开始进行细胞分化,桑椹胚变成囊胚。在子宫中,囊胚周围的透明带分解,允许它在受精后大约6天嵌入子宫壁。着床标志着胚胎形成萌芽阶段的结束。[1]
1.1 囊胚形成
受精卵通过有丝分裂发育,当它发育成16个细胞时,就被称为桑椹胚。在发育的这个阶段之前,所有的细胞(卵裂球)都是自主的,没有特定的命运。在许多动物中,桑椹胚随后通过空化作用发育成囊胚。细胞分化将囊胚细胞发育成两种类型:围绕囊胚腔的滋养层细胞和内细胞团(胚胎)。这个概念后来被称为囊胚。【2】囊胚内细胞团形成的一侧称为动物极,另一侧为植物极。滋养层细胞的外层因致密化而将钠离子泵入囊胚,这使得水通过渗透作用进入并形成内部充满液体的胚泡腔(囊胚腔)。囊胚腔、滋养层细胞和内细胞团细胞是囊胚的标志。[2]
1.2 着床
着床对早期人类胚胎的生存和发展至关重要。它建立了母亲和早期胚胎之间的联系,这种联系将持续整个妊娠的剩余时间。囊胚和子宫内膜壁的结构变化使着床成为可能。[3] 囊胚周围的透明带破裂,称为孵化。这消除了对胚胎块物理大小的限制,并将囊胚的外部细胞暴露于子宫内部。此外,母亲体内的激素变化,特别是黄体生成素(LH)的峰值,使子宫内膜做好接收和包裹囊胚的准备。免疫系统也被调节以允许外来胚胎细胞的入侵。一旦与子宫内膜的细胞外基质结合,滋养层细胞分泌酶和其他因子,将囊胚嵌入子宫壁。释放的酶降解子宫内膜,而自分泌生长因子如人绒毛膜促性腺激素(hCG)和类胰岛素生长因子(IGF)允许囊胚进一步侵入子宫内膜。[4]
着床子宫壁允许胚胎形成的下一步,原肠胚形成,包括从滋养层细胞形成胎盘和将内细胞团分化为羊膜囊和上胚层。
2 结构编辑
卵裂球细胞有两种类型:[5]
- 内细胞团,也称为成胚细胞,产生原始内胚层和胚固有层(上胚层)。
- 原始内胚层发育成羊膜囊,羊膜囊形成充满液体的腔,胚胎在怀孕期间就位于其中。[6]
- 上胚层在原肠胚形成过程中产生发育胚胎的三个胚层(内胚层、中胚层和外胚层)。
- 滋养层是形成囊胚外环的细胞层,囊胚外环与母体子宫内膜结合形成胎盘。滋养层细胞也分泌因子来制造囊胚腔。[7]
- 着床后,细胞滋养层是滋养层的内层,由干细胞组成,产生的细胞包括绒膜绒毛、胎盘和合胞体滋养层。
- 着床后,合胞体滋养层是滋养层的最外层。这些细胞分泌蛋白水解酶分解子宫内膜细胞外基质,使囊胚着床子宫壁。[8]
囊胚腔的流体腔包含氨基酸、生长因子和细胞分化所需的其他分子。[9]
2.1 细胞分化
多个过程控制囊胚中的细胞谱系分化,以产生滋养层、上胚层和原始内胚层。这些过程包括基因表达、细胞信号传导、细胞间接触和位置关系以及表观遗传学。
一旦囊胚内形成了内细胞团,这种细胞团就为进一步分化成上胚层和原始内胚层做好了准备。这一分化过程部分由成纤维细胞生长因子(FGF)信号决定,该信号产生一种改变细胞基因组的磷酸腺苷激酶途径。[10] 卵裂球进一步分离进入滋养层和内细胞团受同源域蛋白Cdx2的调节。这种转录因子抑制滋养层Oct4和Nanog转录因子的表达。[11] 这这些基因组的改变允许在原肠胚形成前的囊胚发育阶段的末期,对上胚层和原始内胚层谱系进行逐步分化。在这些早期胚胎阶段进行的大部分研究是在小鼠胚胎上进行的,哺乳动物之间的特定因子可能不同。
在小鼠中,原始生殖细胞是由上胚层细胞分化而来,这一过程伴随着大量的全基因组表观遗传的重编程。[12] 编程涉及总体脱氧核糖核酸去甲基化和染色质重组,导致细胞的全能性。[12] 全基因组去甲基化的过程包括基于脱氧核糖核酸的切除修复途径。[13]
滋养层细胞在其细胞表面表达整合素,使其能够粘附到子宫壁的细胞外基质上。这种相互作用允许着床并触发进一步分化成三种不同的细胞类型,为囊胚原肠胚形成做准备。[14]
3 临床意义编辑
3.1 妊娠试验
囊胚在着床期间分泌的人绒毛膜促性腺激素水平是妊娠检查中测量的因素。血液和尿液中的绒毛膜促性腺激素都可以测定,以确定妇女是否怀孕。多胎妊娠会分泌更多的人体绒毛膜促性腺激素。人体绒毛膜促性腺激素的血液检测也可以用来检查异常妊娠。[15]
3.2 体外受精
体外受精(IVF)是传统体内受精的一种替代方法,用精子给卵子受精并将胚胎植入女性子宫。多年来,胚胎在受精后两到三天被植入子宫。然而,在发育的这个阶段,很难预测哪个胚胎发育最好,并且通常植入几个胚胎。几个植入的胚胎增加了胎儿发育的可能性,但也可能导致了多个胎儿的发育。这是体外受精中使用胚胎的一个主要问题和缺点。
囊胚用于人类体外受精已被证明是成功的,并且是不能自然受孕的夫妇的常见选择。囊胚是在卵子受精后五到六天植入的。[16] 五六天后,确定哪些胚胎会导致健康的活产就容易多了。知道哪些胚胎会成功,只需植入一个囊胚,就能大幅降低多胎分娩的健康风险和费用。既然胚胎和囊胚发育的营养需求已经确定,就更容易给胚胎提供正确的营养来维持它们进入囊胚阶段。
体外受精后囊胚着床是一个无痛的过程,其中将导管插入阴道,通过超声引导穿过子宫颈,然后进入子宫,在子宫中囊胚被嵌入子宫。
囊胚还提供了一个优势,因为它们可以用来对细胞进行基因测试,以检查基因问题。囊胚中有足够多的细胞,可以在不干扰囊胚发育的情况下除去少量滋养层细胞。这些细胞可以使用胚胎植入前基因筛查(PGS)或特殊形态(如囊胞性纤维症,通常称为胚胎植入前基因诊断(PGD))来检测这些细胞的染色体异倍性。[17]
参考文献
- [1]
^Sherk, Stephanie Dionne (2006). "Prenatal Development". Gale Encyclopedia of Children's Health. Archived from the original on 2013-12-01. Retrieved 2013-12-07..
- [2]
^Gilbert SF. Developmental Biology. 6th edition. Sunderland (MA): Sinauer Associates; 2000. Early Mammalian Development. Available from: https://www.ncbi.nlm.nih.gov/books/NBK10052/.
- [3]
^Zhang, Shuang; Lin, Haiyan; Kong, Shuangbo; Wang, Shumin; Wang, Hongmei; Wang, Haibin; Armant, D. Randall (2013). "Physiological and molecular determinants of embryo implantation". Molecular Aspects of Medicine. 34 (5): 939–80. doi:10.1016/j.mam.2012.12.011. PMC 4278353. PMID 23290997..
- [4]
^Srisuparp, Santha; Strakova, Zuzana; Fazleabas, Asgerally T (2001). "The Role of Chorionic Gonadotropin (CG) in Blastocyst Implantation". Archives of Medical Research. 32 (6): 627–34. doi:10.1016/S0188-4409(01)00330-7. PMID 11750740..
- [5]
^Scott F. Gilbert (15 July 2013). Developmental Biology. Sinauer Associates, Incorporated. ISBN 978-1-60535-173-5.[页码请求].
- [6]
^Schoenwolf, Gary C., and William J. Larsen. Larsen's Human Embryology. 4th ed. Philadelphia: Churchill Livingstone/Elsevier, 2009. Print.[页码请求].
- [7]
^James, J. L; Stone, PR; Chamley, LW (2005). "Cytotrophoblast differentiation in the first trimester of pregnancy: Evidence for separate progenitors of extravillous trophoblasts and syncytiotrophoblast". Reproduction. 130 (1): 95–103. doi:10.1530/rep.1.00723. PMID 15985635..
- [8]
^Vićovac, L; Aplin, JD (1996). "Epithelial-mesenchymal transition during trophoblast differentiation". Acta Anatomica. 156 (3): 202–16. doi:10.1159/000147847. PMID 9124037..
- [9]
^Gasperowicz, M.; Natale, D. R. C. (2010). "Establishing Three Blastocyst Lineages – Then What?". Biology of Reproduction. 84 (4): 621–30. doi:10.1095/biolreprod.110.085209. PMID 21123814..
- [10]
^Yamanaka, Y.; Lanner, F.; Rossant, J. (2010). "FGF signal-dependent segregation of primitive endoderm and epiblast in the mouse blastocyst". Development. 137 (5): 715–24. doi:10.1242/dev.043471. PMID 20147376..
- [11]
^Strumpf, D.; Mao, CA; Yamanaka, Y; Ralston, A; Chawengsaksophak, K; Beck, F; Rossant, J (2005). "Cdx2 is required for correct cell fate specification and differentiation of trophectoderm in the mouse blastocyst". Development. 132 (9): 2093–102. doi:10.1242/dev.01801. PMID 15788452..
- [12]
^Hackett JA, Sengupta R, Zylicz JJ, Murakami K, Lee C, Down TA, Surani MA (January 2013). "Germline DNA demethylation dynamics and imprint erasure through 5-hydroxymethylcytosine". Science. 339 (6118): 448–52. doi:10.1126/science.1229277. PMC 3847602. PMID 23223451..
- [13]
^Hajkova P, Jeffries SJ, Lee C, Miller N, Jackson SP, Surani MA (July 2010). "Genome-wide reprogramming in the mouse germ line entails the base excision repair pathway". Science. 329 (5987): 78–82. doi:10.1126/science.1187945. PMC 3863715. PMID 20595612..
- [14]
^C.H. Damsky; Librach, C; Lim, KH; Fitzgerald, ML; McMaster, MT; Janatpour, M; Zhou, Y; Logan, SK; Fisher, SJ (1994-12-01). "Integrin switching regulates normal trophoblast invasion". Development. 120 (12): 3657–66. PMID 7529679..
- [15]
^"Human Chorionic Gonadotropin (hCG)". WebMD. 2010. Retrieved 2013-12-07..
- [16]
^Fong, C. Y.; Bongso, A.; Ng, S. C.; Anandakumar, C.; Trounson, A.; Ratnam, S. (1997). "Ongoing normal pregnancy after transfer of zona-free blastocysts: Implications for embryo transfer in the human". Human Reproduction. 12 (3): 557–60. doi:10.1093/humrep/12.3.557. PMID 9130759..
- [17]
^Wang, Jeff; Sauer, Mark V (December 2006). "In vitro fertilization (IVF): a review of 3 decades of clinical innovation and technological advancement". Therapeutics and Clinical Risk Management. 2 (4): 355–364. doi:10.2147/tcrm.2006.2.4.355. ISSN 1176-6336. PMC 1936357. PMID 18360648..
暂无