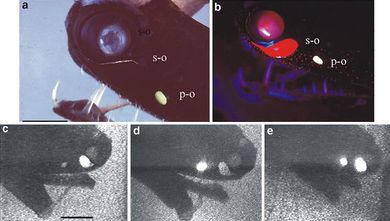
生物发光
编辑生物发光是由活体生物产生和发射的光。它是化学发光的一种形式。生物发光广泛存在于海洋脊椎动物和无脊椎动物,以及一些真菌、微生物,包括一些生物发光细菌和陆地无脊椎动物,如萤火虫。在一些动物中,光是细菌产生的,由共生生物产生,例如弧菌属(Vibrio )细菌;在其他情况下,它是自生的,由动物自己产生。
一般来说,生物发光中的主要化学反应涉及一些发光分子和一种酶,通常分别称为萤光素和萤光素酶。因为这些是通用名,萤光素和萤光素酶通常通过包括种类或组来区分,即萤火虫萤光素。在所有表征的情况下,酶催化萤光素的氧化。
在某些物种中,萤光素酶需要其他辅因子,如钙或镁离子,有时还需要携带能量的分子三磷酸腺苷(ATP)。在进化过程中,萤光素变化很小:特别是一种,腔肠素,在11种不同的动物(门)中发现,尽管在其中一些动物通过它们的饮食获得它。相反,萤光素酶在不同物种之间差异很大,因此生物发光在进化史中出现了40多次。
亚里士多德(Aristotle)和老普林尼(Pliny the Elder)都提到潮湿的木头有时会发光,许多世纪后,罗伯特·波义耳( Robert Boyle)证明氧气参与了这个过程,包括木头和发光蠕虫。直到19世纪晚期,生物发光才得到正确的研究。这种现象在动物群体中广泛分布,特别是在海洋环境中,鞭毛藻在水的表层引起磷光。在陆地上,它发生在真菌、细菌和一些无脊椎动物群体中,包括昆虫。
动物对生物发光的利用包括反照明伪装、模仿其他动物,例如引诱猎物,以及向同一物种的其他个体发出信号,例如吸引配偶。在实验室,萤光素酶系统被用于基因工程和生物医学研究。其他研究人员正在研究将生物发光系统用于街道照明和装饰照明的可能性,并且已经创建了一个生物发光植物。[1]
目录编辑
1 历史编辑
在煤矿用安全灯出现之前,干鱼皮在英国和欧洲被用作微弱的光源。[2] 这种实验形式的照明避免了使用蜡烛的必要性,蜡烛有引发沼气爆炸的危险。[3] 矿井中另一个安全的照明来源是装有萤火虫的瓶子。[4] 1920年,美国动物学家牛顿·哈维( E. Newton Harvey)出版了一部专著, 动物之光的本质(The Nature of Animal Light),总结了生物发光的早期研究工作。哈维指出亚里士多德提到死鱼和肉产生的光,亚里士多德和老普林尼(在他的 自然历史)提到潮湿木头发出的光。他还记录了罗伯特·波义耳对这些光源的实验,并表明它们和发光蠕虫都需要空气来产生光。哈维指出,1753年,贝克(J. Baker)发现了鞭毛虫 夜光虫(Noctiluca) “作为一种发光的动物”“肉眼就能看见”,[5] 1854年,约翰·弗洛里安·黑勒( Johann Florian Heller, 1813-1871)发现真菌的菌丝是枯木中的光源。[6]
塔克(Tuckey)在他死后的1818年出版的 扎伊尔探险的叙述(Narrative of the Expedition to the Zaire)中描述了捕捉发光的动物。他提到透明、甲壳类动物(他把水的乳白色归因于它们)和螃蟹(虾和蟹)。在显微镜下,他描述了大脑中的“发光特性”,类似于“一个在脑中的大头针头大小的最明亮的紫水晶”。[7]
查尔斯·达尔文(Charles Darwin)注意到海洋中的生物发光,并在他的日记(Journal)中记录以下内容:
当我在漆黑的夜幕下的这些纬度地区航行时,海洋呈现出一种最美丽和惊艳的壮观镜像。当一阵凉爽的风吹过,在白天看起来像是泡沫的所有海面,此时发出苍白的微光。行驶的船在她船头两侧激起液态磷一样的两道浪花,在她的船尾航迹中像是跟着一辆乳白色的火车。在目之所见的范围内,每一道浪花的弧顶都是明亮的。与其他部分的天空比起来,在海平线上的天空,从这些紫青色的火焰中的反光里, 看起来并不是完全模糊的。[8]
达尔文还观察到一种发光的“Dianaea属水母”[8] 并指出“当波浪闪烁着明亮的绿色火花时,我相信这通常是因为微小的甲壳纲动物。但毫无疑问,许多其他远洋动物活着的时候都发出磷光。”[8] 他猜测“受到干扰的大气层带电情况”[8] 可能与此有关。丹尼尔·波利(Daniel Pauly)评论道,达尔文“幸运地猜对了大部分,但不是在这里”, 注意到当时生物化学知识的匮乏,以及所涉及的海洋动物的复杂进化“太令人不安了”。
生物发光在冷战中引起了美国海军的注意,因为潜艇在一些水域可以产生足够明亮的尾流以被探测到;一艘德国潜艇在第一次世界大战中被击沉,正是以这种方式被发现的。海军感兴趣的是预测何时这种探测是可能的,从而指导他们自己的潜艇避免被探测到。
在生物发光导航的轶事中,阿波罗13号宇航员吉姆·洛威尔(Jim Lovell)讲述了作为一名海军飞行员,他的导航系统失灵时,他是如何回到自己的航空母舰香格里拉号(USS Shangri-La)的。关掉机舱灯,他看到了船发光的尾流,并能够飞到船上安全着陆。[9]
法国药理学家拉斐尔·杜布瓦(Raphaël Dubois)在19世纪末进行了生物发光的研究。他研究磕头虫(Pyrophorus)和海洋双壳软体动物海笋(Pholas dactylus)。他驳斥了生物发光来自磷的旧观点,[10] 并证明了这一过程与一种特定化合物被酶氧化有关,他称之为萤光素。[11] 他把保存在糖里的软体动物的虹吸管送给哈维。哈维对生物发光产生了兴趣,因为他参观了南太平洋和日本,并在那里观察到磷光生物。他研究这个现象很多年了。他的研究旨在证明萤光素和作用于萤光素的酶产生光,在物种之间是可以互换的,表明所有生物发光有机体都有一个共同的祖先。然而,他发现这个假设是错误的,不同的生物体在发光蛋白质的组成上有很大的差异。接下来的三十年里,他一直在提纯和研究这些成分,但是年轻的日本化学家下村修(Osamu Shimomura)第一个获得结晶萤光素。他用了海洋萤火虫 希氏弯喉海萤(Vargula hilgendorfii),但又过了十年,他才发现了这种化学物质的结构,并能够发表他1957年的论文 结晶海萤属萤光素(Crystalline Cypridina Luciferin)。 最近,马丁·查尔菲(Martin Chalfie)、下村修和钱永健(Roger Y. Tsien)因他们在1961年发现和开发绿色荧光蛋白作为生物研究工具而获得了2008年诺贝尔化学奖。[12]
哈维在1957年写了一份关于所有发光形式的详细历史记录。[13] 最近出版了一本关于生物发光的最新书籍,也涵盖了二十世纪和二十一世纪初的相关研究。[14]
2016年,深海生物发光珊瑚首次在彩色高清视频中被拍摄到。[15]
2 进化编辑
E. N. 哈维(1932)是第一批提出生物发光如何进化的人之一。[16] 在这篇早期的论文中,他提出原始生物发光可能来自于含有荧光基团的呼吸链蛋白。这一假设后来被否定了,但它确实引起了人们对这一现象起源的极大兴趣。今天,两个流行的假说(都与海洋生物发光有关)是由塞利格(Seliger)(1993)和里斯(Rees)等人(1998)提出的。[17][18]
塞利格的理论认为萤光素酶是生物发光系统进化的催化剂。这表明萤光素酶的最初目的是作为混合功能加氧酶。随着许多物种的早期祖先进入更深更暗的水域,自然选择施加了有利于提高眼睛敏感度和增强视觉信号的力量。[19] 如果选择倾向于色素分子(通常与吸引配偶或分散捕食者注意力的斑点相关的分子)分解所需的加氧酶突变,最终可能导致组织的外部发光。[17]
里斯等人(1998年)利用从海洋萤光素:腔肠素收集的证据表明,对萤光素起作用的选择可能是由于保护海洋生物免受潜在有害活性氧的压力(例如H2O2 O2− )。当抗氧化防御的选择强度随着早期物种进一步向水体柱下方移动而降低时,可能发生从抗氧化到生物发光的功能转变。在更深的深度,活性氧的暴露明显更低,通过新陈代谢内源性产生活性氧也是如此。[18]
虽然起初很受欢迎,但塞利格的理论受到了挑战,特别是在里斯研究的生化和基因证据上。然而,仍然清楚的是,生物发光已经独立进化了至少40次。[20] 鱼类的生物发光至少始于白垩纪。已知约有1500种鱼类是生物发光的;鱼类的这种能力至少独立进化了27次。在这27个场合中,17个涉及从周围水中吸收生物发光细菌,而在其他场合中,内在的光通过化学合成而进化。这些鱼在深海中变得惊人地多样化,并借助它们的神经系统控制它们的光,不仅用来引诱猎物或躲避捕食者,还用来交流。[21][22]
所有生物发光有机体都有一个共同点。荧光素酶总是催化荧光素和氧气发光。[23] 麦克罗伊(McElroy)和塞利格在1962年提出,生物发光反应进化为解除氧气的毒性。所以生物发光与光合生物平行进化。[24] 今天,生物发光还有其他用途。
3 化学机理编辑
生物发光是一种化学发光形式,光能通过化学反应释放出来。该反应涉及发光颜料萤光素和萤光素酶酶组分。 由于萤光素/萤光素酶组合的多样性,在化学机理上几乎没有共同点。从目前的研究系统来看,唯一统一的机制是分子氧的作用,尽管许多例子同时释放二氧化碳。例如,萤火虫萤光素/萤光素酶反应需要镁和三磷酸腺苷,并产生二氧化碳(CO2),一磷酸腺苷和焦磷酸作为废弃产物。反应可能需要其他辅因子,如钙离子(Ca2+)之于水母发光蛋白,或镁离子(Mg2+)和三磷酸腺苷用于萤火虫萤光素酶。[25] 一般来说,这种反应可以描述为:
水晶果冻水母(Aequorea victoria) 利用另一种称为发光蛋白的蛋白质代替萤光素酶,具体而言是水母发光蛋白。[26] 当加入钙离子时,快速催化会产生短暂的闪光,这与萤光素酶产生的持久辉光截然不同。在第二个更慢的步骤中,萤光素从氧化(氧化萤光素)形式再生,使其与水母发光蛋白重组,为后续的闪光做好准备。因此,发光蛋白是酶,但具有不同寻常的反应动力学。[27] 此外,水母发光蛋白与钙离子接触释放的一些蓝光被绿色荧光蛋白吸收,而绿色荧光蛋白又在共振能量转移过程中释放绿光。[28]
总的来说,生物发光在进化史中已经出现了四十多次。 在进化过程中,萤光素的变化很小:尤其是腔肠素,是九个门(几种非常不同的生物)的发光色素,包括多囊类放射虫、丝足虫(稀孔虫)、原生动物、栉水母、刺胞动物(包括水母和珊瑚)、甲壳类动物、软体动物、箭虫和脊椎动物(鳍刺类鱼)。并非所有这些生物都合成腔肠素:其中一些是通过饮食获得的。 相反,萤光素酶变化很大,并且在每个物种中往往不同。
4 分布编辑
生物发光广泛存在于动物中,尤其是在远海,包括鱼类、水母、栉水母、甲壳类动物和头足类软体动物;一些真菌和细菌;以及包括昆虫在内的许多陆地无脊椎动物。大约76%的深海动物主要分类群产生光。[29] 大多数海洋光发射在蓝色和绿色光谱中。然而,一些松颌鱼会发出红光和红外光,浮蚕(Tomopteris) 发出黄光。[30][30]
最常见的生物发光生物可能是海洋表层的鞭毛藻,这是夜间在受干扰的水中有时会出现闪光磷光的原因。至少有18个属能够发光。[30] 另一种不同的效应是数千平方英里的海洋,它们被生物发光细菌产生的光照射,这种效应被称为马雷效应或乳状海洋效应。[31]
非海洋生物发光分布不太广泛,两个最著名的例子是萤火虫和发光蠕虫。包括昆虫幼虫、环节动物和蛛形纲动物在内的其他无脊椎动物具有生物发光的能力。某些形式的生物发光在夜间更亮(或只存在于夜间),遵循昼夜节律。
5 在自然界的用途编辑
生物发光在不同的分类群中有几种功能。史蒂文·哈德克(Steven Haddock)等人(2010年)将以下功能或多或少地列为海洋生物的明确功能:打草惊蛇的防御功能、反光照(伪装)、误导(烟幕)、分散注意力的身体部位、猎物警报(使捕食者更容易被更高级的捕食者看到),以及威慑其他动物的警告;引诱、击昏或迷惑猎物等攻击功能、照亮猎物和吸引/识别配偶。对研究人员来说,检测一个物种能够产生光要比分析化学机制或证明光的功能容易得多。[32] 在某些情况下,这种功能是未知的,例如蚯蚓(寡毛纲)的三个科的物种,例如 Diplocardia longa 移动时体腔液会发光。[32] 下列功能在命名的生物体中已经相当确定。
5.1 反光照伪装
在深海的许多动物中,包括几个乌贼物种,细菌生物发光被用于反光照伪装,从下面看,动物与头顶的环境光线相匹配。[33] 在这些动物中,光感受器控制发光以匹配背景的亮度。[33] 这些发光器官通常与含有生物发光细菌的组织有所区别。然而,在夏威夷短尾乌贼(Euprymna scolopes)中,细菌是动物完整发光器官的组成部分。[34]
5.2 吸引
一种来自新西兰的蕈蚊,小真菌蚋(Arachnocampa luminosa),生活在没有捕食者的洞穴环境中,它的幼虫发出蓝绿色的光。[35] 它们悬挂着发光并吸引飞虫的丝线,当猎物被缠住时,它们缠绕在线上。[36] 生活在河岸和悬岩下的另一种北美蕈蚊幼虫的生物发光也有类似的功能。 Orfelia fultoni 构建粘粘的小网,发出深蓝色的光。它有一个内置的生物钟,即使在完全黑暗的情况下,它也能按照昼夜节律打开和关闭发光。[37]
萤火虫用光来吸引配偶。根据物种,涉及两个系统;一种是,雌性从腹部发光来吸引雄性;另一方面,飞行的雄性会发出信号,有时静止的雌性会做出反应。[32][37] 磕头虫在飞行时会从腹部发出橙色光,在地面上受到干扰或移动时会从胸部发出绿色光。前者可能是性引诱剂,但后者可能是防御性的。[32] 磕头虫 Pyrophorus nyctophanus 的幼虫生活在巴西的白蚁丘的表层。它们通过发出明亮的绿色光来照亮土丘,吸引它们赖以为生的飞虫。[32]
在海洋环境中,利用发光吸引配偶主要是介形类动物、小型虾状甲壳类动物,尤其是鲤科动物。信息素可用于远距离通讯,生物发光可用于近距离,使配偶能够“回家”。[32] 百慕大萤火虫是一种多毛类蠕虫,在满月后的几个晚上,当雌性发光吸引雄性时,它会做一个简短的展示。[38]
5.3 防卫
许多头足类动物,包括至少70个乌贼属,都是生物发光的。[32] 一些乌贼和小型甲壳动物使用生物发光化学混合物或细菌浆,就像许多乌贼使用墨水一样。当动物逃到安全的地方时,一团发光物质被排出,排斥潜在的捕食者或分散它的注意力。[32] 深海乌贼 八腕鱿鱼(Octopoteuthis deletron)可能会自动切除其手臂发光的部分,并继续抽动和闪光,从而在逃跑时分散捕食者的注意力。[32]
双鞭毛藻可能利用生物发光来防御捕食者。当它们发现捕食者时会发光,这可能会吸引高级捕食者的注意力,使捕食者本身变得更加容易受到伤害。[32] 放牧桡足类动物释放任何闪光无害的浮游植物细胞;如果被吃掉,它们会让桡足类发光,吸引捕食者,所以浮游植物的生物发光是防御性的。食肉性深海鱼类的胃内容物发光的问题得到了解决(这一解释得到了证实):它们的胃有一层黑色的衬里,能够阻挡任何生物发光的鱼猎物发出的光,这些被吞下的鱼猎物是为了吸引更大的捕食者而发光。[39]
海萤是一种生活在沉积物中的小型甲壳动物。静止时,它会发出暗淡的光,但当受到干扰时,它会迅速离去,留下一团闪烁的蓝光来迷惑捕食者。第二次世界大战期间,它被收集起来晒干,供日本军方在秘密行动中用作光源。[39]
铁路蠕虫的幼虫(Phrixothrix)在每个身体部分具有成对的光器官,能够用绿光发光;这些被认为有防御目的。[39] 他们头上也有能发出红光的器官;它们是唯一发出这种颜色光的陆生动物。[40]
5.4 警告
警戒色是生物发光的一个广泛应用的功能,它提供了一个警告,令相关生物产生难以接受的感觉。有人认为许多萤火虫幼虫通过发光来击退捕食者;一些千足虫发出同样的光。[41] 一些海洋生物被认为出于类似的原因发光。这些包括鳞虫、水母和海蛇尾,但是需要进一步的研究来完全建立发光功能的研究体系。如果软体刺胞动物能够以这种方式阻止捕食,这种机制将对它们特别有利。[32] 冒贝 Latia neritoides 是已知唯一会发光的淡水腹足动物。它产生绿色发光粘液,可能具有反捕食者的功能。[42] 海洋蜗牛 巴西海蜗牛(Hinea brasiliana) 使用闪光,可能是为了阻止捕食者。蓝绿色的光通过半透明的外壳发射出去,半透明的外壳起到有效的光漫射器的作用。[43]
5.5 沟通
群体感应形式的交流在许多细菌物种的发光调节中发挥作用。当细胞密度(通过分泌分子的浓度来衡量)很高时,细胞外分泌的小分子会刺激细菌开启发光基因。[32]
鳞海鞘是群体被囊动物,每个动物体在入口虹吸管的两侧都有一对发光器官。当受到光刺激时,这些开关会打开和关闭,导致有节奏的闪烁。动物体之间没有神经通路,但是每一个都对其他个体产生的光有反应,甚至对附近其他群体的光也有反应。[44] 动物体之间通过光发射的交流可以协调群体的努力,例如在游泳中,每个动物体提供部分推进力。[45]
一些生物发光细菌感染寄生在鳞翅目幼虫身上的线虫。当这些毛虫死去时,它们的发光度可能会吸引掠食者来捕食死去的昆虫,从而有助于细菌和线虫的传播。[32] 一个相似的原因可能解释了许多发光真菌的种类的发光现象。属中的物种 蜜环菌属 (Armillaria), 小菇属(Mycena), 类脐菇属(Omphalotus), 扇菇属(Panellus), 侧耳属(Pleurotus)等其他真菌也有这种现象,通常从菌丝、菌伞和菌褶发出绿色的光。这可能会吸引夜间飞行的昆虫帮助孢子扩散,但也可能涉及其他功能。[32]
Quantula striata 是唯一已知的生物发光陆生软体动物。光脉冲是从脚前部附近的腺体发出的,可能具有交流功能,尽管适应的意义还没有完全理解。[46]
5.6 模仿
生物发光被各种动物用来模仿其他物种。许多种类的深海鱼类,如𩽾𩾌鱼和龙鱼,利用攻击性模仿来吸引猎物。它们头上有一个叫做esca的附属物,内含生物发光细菌,能够产生鱼可以控制的持久发光。发光的esca被摇晃或挥动,以引诱小动物靠近鱼的攻击距离。[32][47]
雪茄达摩鲨利用生物发光通过反光照来伪装其下侧,但其胸鳍附近的一小块区域仍然是黑暗的,对于在它下面游动的金枪鱼和鲭鱼等大型食肉鱼来说,它就像一条小鱼。当这种鱼接近诱饵时,它们被鲨鱼咬了。[48][49]
雌性的 Photuris 萤火虫有时模仿另一种北美萤火虫的光模式,吸引后者的雄性作为猎物。通过这种方式,他们获得了Photuris 无法合成的食物和防御性化学物质lucibufagins,。[50]
南美巨型蟑螂属 Lucihormetica 被认为是第一个已知的防御性模仿的例子,发出光来模仿有毒磕头虫的生物发光。[51] 然而,人们对这一说法产生了怀疑,并且没有确凿的证据表明蟑螂是生物发光的。[52][53]
5.7 照明
虽然大多数海洋生物发光是绿色到蓝色,但一些深海触须龙鱼属奇巨口鱼属(Aristostomias), 厚巨口鱼属(Pachystomias) 和 柔骨鱼属(Malacosteus) 发出红光。这种适应使鱼能够看到红色的猎物,在深水环境中红色的光被水体柱过滤掉,这些猎物通常是看不见的。[54]
黑龙鱼(也叫北红灯松颌鱼) 黑柔骨鱼( Malacosteus niger ) 被认为是唯一发出红光的鱼。然而,它的眼睛对这种波长不敏感;它还有一种额外的视网膜色素,当被照亮时会发出蓝绿色荧光。这提醒鱼注意猎物的存在。这种额外的色素被认为是从桡足类中发现的叶绿素衍生物中吸收的,桡足类是黑柔骨鱼食物的一部分。[55]
6 生物技术编辑
6.1 生物学和医学
生物发光生物是许多研究领域的目标。萤光素酶系统在基因工程中被广泛用作报告基因,每一个都通过荧光产生不同的颜色,[56][57] 以及使用生物发光成像的生物医学研究。[58][59][60] 例如,萤火虫萤光素酶基因早在1986年就被用于转基因烟草植物的研究。[61] 弧菌 与海洋无脊椎动物如夏威夷短尾乌贼(Euprymna scolopes)共生,是生物发光的关键实验模型。[62][63] 生物发光激活破坏是一种实验性癌症治疗方法。[64] 另请参阅光遗传学,它涉及使用光来控制活组织中的细胞,通常是神经元,这些细胞已被基因修饰以表达光敏离子通道,还请参阅生物光子,生物光子是从生物系统发出的可见光谱和紫外光谱中的非热源光子。
6.2 光的产生
工业设计者正在研究发光器的结构,发光器是生物发光生物中的发光器官。工程生物发光也许有一天可以用来减少对街道照明的需求,或者用于装饰目的,如果有可能产生足够亮并且可以以可行的价格长期维持的光。[65][65][66] 让萤火虫的尾巴发光的基因已经被添加到芥菜植物中。植物被触摸时会微弱发光一个小时,但是需要一台灵敏的照相机才能看到这种发光。[67] 威斯康星大学麦迪逊分校正在研究利用基因工程进行生物发光大肠杆菌作为灯泡中的生物发光细菌。[68] 2011年,飞利浦推出了家庭环境照明微生物系统。[69][70] 剑桥(英国)的iGEM团队已经开始解决萤光素在发光反应中被消耗的问题,方法是开发一个基因生物技术部分,该部分编码来自北美萤火虫的萤光素再生酶;这种酶“有助于增强和维持光输出”。[71] 2016年,法国公司Glowee开始销售生物发光灯,将店面和市政街道标志作为主要市场。[72] 法国有一项法律禁止零售商和办公室在凌晨1点到7点之间照明窗户,以最大限度地减少能源消耗和污染。[73][74] Glowee希望他们的产品能绕过这项禁令。他们使用了一种叫做 Aliivibrio fischeri 在黑暗中发光,但是他们产品的最长寿命是三天。[72]
参考文献
- [1]
^Callaway, E. 2013. Glowing plants spark debate. Nature, 498:15–16, 04 June 2013. http://www.nature.com/news/glowing-plants-spark-debate-1.13131.
- [2]
^Smiles, Samuel (1862). Lives of the Engineers. Volume III (George and Robert Stephenson). London: John Murray. p. 107. ISBN 978-0-7153-4281-7. (ISBN refers to the David & Charles reprint of 1968 with an introduction by L. T. C. Rolt).
- [3]
^Freese, Barbara (2006). Coal: A Human History. Arrow. p. 51. ISBN 978-0-09-947884-3..
- [4]
^Fordyce, William (20 July 1973). A history of coal, coke and coal fields and the manufacture of iron in the North of England. Graham..
- [5]
^Harvey cites this as Baker, J.: 1743–1753, The Microscope Made Easy and Employment for the Microscope..
- [6]
^Harvey, E. Newton (1920). The Nature of Animal Light. Philadelphia & London: J. B. Lippencott. Page 1..
- [7]
^Tuckey, James Hingston (May 1818). Thomson, Thomas, ed. Narrative of the Expedition to the Zaire. Annals of Philosophy. volume XI. p. 392. Retrieved 22 April 2015..
- [8]
^Darwin, Charles (1839). Narrative of the surveying voyages of His Majesty's Ships Adventure and Beagle between the years 1826 and 1836, describing their examination of the southern shores of South America, and the Beagle's circumnavigation of the globe. Journal and remarks. 1832–1836. Henry Colburn. pp. 190–192..
- [9]
^Huth, John Edward (15 May 2013). The Lost Art of Finding Our Way. Harvard University Press. p. 423. ISBN 978-0-674-07282-4..
- [10]
^Reshetiloff, Kathy (1 July 2001). "Chesapeake Bay night-lights add sparkle to woods, water". Bay Journal. Retrieved 16 December 2014..
- [11]
^Poisson, Jacques (April 2010). "Raphaël Dubois, from pharmacy to bioluminescence". Rev Hist Pharm (Paris) (in French). 58 (365): 51–56. ISSN 0035-2349. PMID 20533808.CS1 maint: Unrecognized language (link).
- [12]
^"The Nobel Prize in Chemistry 2008". 8 October 2008. Retrieved 23 November 2014..
- [13]
^Harvey, E. Newton (1957). A History of Luminescence: From the Earliest Times Until 1900. Philadelphia: American Philosophical Society..
- [14]
^Anctil, Michel (2018). Luminous Creatures: The History and Science of Light Production in Living Organisms. Montreal & Kingston, London, Chicago: McGill-Queen's University Press. ISBN 978-0-7735-5312-5..
- [15]
^Taylor, Liz (9 Aug 2016). "Deep Sea Bioluminescent Corals Captured for the First Time in Color HD Video". National Geographic. National Geographic. Retrieved 9 Aug 2016..
- [16]
^Harvey, E.N. (1932). "The evolution of bioluminescence and its relation to cell respiration". Proceedings of the American Philosophical Society. 71: 135–141..
- [17]
^Seliger, H.H. (1993). "Bioluminescence: excited states under cover of darkness". Naval Research Reviews. 45..
- [18]
^Rees, J. F.; et al. (1998). "The origins of marine bioluminescence: Turning oxygen defence mechanisms into deep-sea communication tools". Journal of Experimental Biology. 201: 1211–1221..
- [19]
^Widder, Edith A. (1999). Archer, S.; Djamgoz, M.B.; Loew, E.; Partridge, J.C.; Vallerga, S., eds. Bioluminescence. Adaptive Mechanisms in the Ecology of Vision. Springer. pp. 555–581..
- [20]
^Haddock, S. H. D.; et al. (2010). "Bioluminescence in the Sea". Annual Review of Marine Science. 2: 443–493. Bibcode:2010ARMS....2..443H. doi:10.1146/annurev-marine-120308-081028. PMID 21141672..
- [21]
^Davis, Matthew P.; Sparks, John S.; Smith, W. Leo (June 2016). "Repeated and Widespread Evolution of Bioluminescence in Marine Fishes". PLoS ONE. 11 (6): e0155154. Bibcode:2016PLoSO..1155154D. doi:10.1371/journal.pone.0155154. PMC 4898709. PMID 27276229..
- [22]
^Yong, Ed (8 June 2016). "Surprising History of Glowing Fish". Phenomena. National Geographic. Retrieved 11 June 2016..
- [23]
^Wilson, Thérèse; Hastings, J. Woodland (1998). "Bioluminescence". Annual Review of Cell and Developmental Biology. 14 (1): 197–230. doi:10.1146/annurev.cellbio.14.1.197. PMID 9891783..
- [24]
^McElroy, William D.; Seliger, Howard H. (December 1962). "Biological Luminescence". Scientific American. 207 (6): 76–91. doi:10.1038/scientificamerican1262-76. ISSN 0036-8733..
- [25]
^Hastings, J.W. (1983). "Biological diversity, chemical mechanisms, and the evolutionary origins of bioluminescent systems". J. Mol. Evol. 19 (5): 309–21. Bibcode:1983JMolE..19..309H. doi:10.1007/BF02101634. ISSN 1432-1432. PMID 6358519..
- [26]
^Shimomura, O.; Johnson, F.H.; Saiga, Y. (1962). "Extraction, purification and properties of aequorin, a bioluminescent protein from the luminous hydromedusan, Aequorea". J Cell Comp Physiol. 59 (3): 223–39. doi:10.1002/jcp.1030590302. PMID 13911999..
- [27]
^Shimomura, O.; Johnson, F.H. (1975). "Regeneration of the photoprotein aequorin". Nature. 256 (5514): 236–238. Bibcode:1975Natur.256..236S. doi:10.1038/256236a0. PMID 239351..
- [28]
^Morise, H.; Shimomura, O.; Johnson, F.H.; Winant, J. (1974). "Intermolecular energy transfer in the bioluminescent system of Aequorea". Biochemistry. 13 (12): 2656–62. doi:10.1021/bi00709a028. PMID 4151620..
- [29]
^Martini, Séverine; Haddock, Steven H. D. (April 2017). "Quantification of bioluminescence from the surface to the deep sea demonstrates its predominance as an ecological trait". Scientific Reports. 7: 45750. Bibcode:2017NatSR...745750M. doi:10.1038/srep45750. PMC 5379559. PMID 28374789..
- [30]
^Sparks, John S.; Schelly, Robert C.; Smith, W. Leo; Davis, Matthew P.; Tchernov, Dan; Pieribone, Vincent A.; Gruber, David F. (8 January 2014). "The Covert World of Fish Biofluorescence: A Phylogenetically Widespread and Phenotypically Variable Phenomenon". PLoS ONE. 9 (1): e83259. Bibcode:2014PLoSO...983259S. doi:10.1371/journal.pone.0083259. PMC 3885428. PMID 24421880..
- [31]
^Ross, Alison (27 September 2005). "'Milky seas' detected from space". BBC. Retrieved 13 March 2013..
- [32]
^Haddock, Steven H.D.; Moline, Mark A.; Case, James F. (2010). "Bioluminescence in the Sea". Annual Review of Marine Science. 2: 443–493. Bibcode:2010ARMS....2..443H. doi:10.1146/annurev-marine-120308-081028. PMID 21141672..
- [33]
^Young, R.E.; Roper, C.F. (1976). "Bioluminescent countershading in midwater animals: evidence from living squid". Science. 191 (4231): 1046–8. Bibcode:1976Sci...191.1046Y. doi:10.1126/science.1251214. PMID 1251214..
- [34]
^Tong, D; Rozas, N.S.; Oakley, T.H.; Mitchell, J.; Colley, N.J.; McFall-Ngai, M.J. (2009). "Evidence for light perception in a bioluminescent organ". Proceedings of the National Academy of Sciences of the United States of America. 106 (24): 9836–41. Bibcode:2009PNAS..106.9836T. doi:10.1073/pnas.0904571106. PMC 2700988. PMID 19509343..
- [35]
^Meyer-Rochow, Victor Benno (2007). "Glowworms: a review of "Arachnocampa" spp and kin". Luminescence. 22 (3): 251–265. doi:10.1002/bio.955. PMID 17285566..
- [36]
^Broadley, R.; Stringer, I. (2009). "Larval behaviour of the New Zealand glowworm, Arachnocampa luminosa (Diptera: Keroplatidae), in bush and caves". In Meyer-Rochow, V.B. Bioluminescence in Focus. Research Signpost: Kerala. pp. 325–355..
- [37]
^Fulcher, Bob. "Lovely and Dangerous Lights" (PDF). Tennessee Conservationist Magazine. Archived from the original (PDF) on 14 August 2014. Retrieved 28 November 2014..
- [38]
^Shimomura, Osamu (2012). Bioluminescence: Chemical Principles and Methods. World Scientific. p. 234. ISBN 978-981-4366-08-3..
- [39]
^Pauly, Daniel (13 May 2004). Darwin's Fishes: An Encyclopedia of Ichthyology, Ecology, and Evolution. Cambridge University Press. pp. 15–16. ISBN 978-1-139-45181-9..
- [40]
^Viviani, Vadim R.; Bechara, Etelvino J.H. (1997). "Bioluminescence and Biological Aspects of Brazilian Railroad-Worms (Coleoptera: Phengodidae)". Annals of the Entomological Society of America. 90 (3): 389–398. doi:10.1093/aesa/90.3.389..
- [41]
^Marek, Paul; Papaj, Daniel; Yeager, Justin; Molina, Sergio; Moore, Wendy (2011). "Bioluminescent aposematism in millipedes". Current Biology. 21 (18): R680–R681. doi:10.1016/j.cub.2011.08.012. PMC 3221455. PMID 21959150..
- [42]
^Meyer-Rochow, V. B.; Moore, S. (1988). "Biology of Latia neritoides Gray 1850 (Gastropoda, Pulmonata, Basommatophora): the Only Light-producing Freshwater Snail in the World". Internationale Revue der Gesamten Hydrobiologie und Hydrographie. 73 (1): 21–42. doi:10.1002/iroh.19880730104..
- [43]
^Deheyn, Dimitri D.; Wilson, Nerida G. (2010). "Bioluminescent signals spatially amplified by wavelength-specific diffusion through the shell of a marine snail". Proceedings of the Royal Society. 278 (1715): 2112–2121. doi:10.1098/rspb.2010.2203. PMC 3107627..
- [44]
^Bowlby, Mark R.; Edith Widder; James Case (1990). "Patterns of stimulated bioluminescence in two pyrosomes (Tunicata: Pyrosomatidae)". Biological Bulletin. 179 (3): 340–350. doi:10.2307/1542326. JSTOR 1542326. PMID 29314963..
- [45]
^Encyclopedia of the Aquatic World. Marshall Cavendish. January 2004. p. 1115. ISBN 978-0-7614-7418-0..
- [46]
^Copeland, J.; Daston, M.M. (1989). "Bioluminescence in the terrestrial snail Quantula (Dyakia) striata". Malacologia. 30 (1–2): 317–324..
- [47]
^Young, Richard Edward (October 1983). "Oceanic Bioluminescence: an Overview of General Functions". Bulletin of Marine Science. 33 (4): 829–845..
- [48]
^Martin, R. Aidan. "Biology of Sharks and Rays: Cookiecutter Shark". ReefQuest Centre for Shark Research. Retrieved 13 March 2013..
- [49]
^Milius, S. (1 August 1998). "Glow-in-the-dark shark has killer smudge". Science News. Retrieved 13 March 2013..
- [50]
^Eisner, Thomas; Goetz, Michael A.; Hill, David E.; Smedley, Scott R.; Meinwald, Jarrold (1997). "Firefly "femmes fatales" acquire defensive steroids (lucibufagins) from their firefly prey". Proceedings of the National Academy of Sciences of the United States of America. 94 (18): 9723–9728. Bibcode:1997PNAS...94.9723E. doi:10.1073/pnas.94.18.9723. PMC 23257. PMID 9275191..
- [51]
^Sullivan, Rachel. "Out of the darkness". ABC Science. Retrieved 17 December 2014..
- [52]
^Greven, Hartmut; Zwanzig, Nadine (2013). "Courtship, Mating, and Organisation of the Pronotum in the Glowspot Cockroach Lucihormetica verrucosa (Brunner von Wattenwyl, 1865) (Blattodea: Blaberidae)". Entomologie Heute. 25: 77–97..
- [53]
^Merritt, David J. (2013). "Standards of evidence for bioluminescence in cockroaches". Naturwissenschaften. 100 (7): 697–698. Bibcode:2013NW....100..697M. doi:10.1007/s00114-013-1067-9. PMID 23740173..
- [54]
^Douglas, R.H.; Mullineaux, C.W.; Partridge, J.C. (29 September 2000). "Long-wave sensitivity in deep-sea stomiid dragonfish with far-red bioluminescence: evidence for a dietary origin of the chlorophyll-derived retinal photosensitizer of Malacosteus niger". Philosophical Transactions of the Royal Society B. 355 (1401): 1269–1272. doi:10.1098/rstb.2000.0681. PMC 1692851. PMID 11079412..
- [55]
^Bone, Quentin; Moore, Richard (1 February 2008). Biology of Fishes. Taylor & Francis. pp. 8: 110–111. ISBN 978-1-134-18630-3..
- [56]
^Koo, J.; Kim, Y.; Kim, J.; Yeom, M.; Lee, I. C.; Nam, H. G. (2007). "A GUS/Luciferase Fusion Reporter for Plant Gene Trapping and for Assay of Promoter Activity with Luciferin-Dependent Control of the Reporter Protein Stability". Plant and Cell Physiology. 48 (8): 1121–31. doi:10.1093/pcp/pcm081. PMID 17597079..
- [57]
^Nordgren, I. K.; Tavassoli, A. (2014). "A bidirectional fluorescent two-hybrid system for monitoring protein-protein interactions". Molecular BioSystems. 10 (3): 485–490. doi:10.1039/c3mb70438f. PMID 24382456..
- [58]
^Xiong, Yan Q.; Willard, Julie; Kadurugamuwa, Jagath L.; Yu, Jun; Francis, Kevin P.; Bayer, Arnold S. (2004). "Real-Time in Vivo Bioluminescent Imaging for Evaluating the Efficacy of Antibiotics in a Rat Staphylococcus aureus Endocarditis Model". Antimicrobial Agents and Chemotherapy. 49 (1): 380–7. doi:10.1128/AAC.49.1.380-387.2005. PMC 538900. PMID 15616318..
- [59]
^Di Rocco, Giuliana; Gentile, Antonietta; Antonini, Annalisa; Truffa, Silvia; Piaggio, Giulia; Capogrossi, Maurizio C.; Toietta, Gabriele (1 September 2012). "Analysis of biodistribution and engraftment into the liver of genetically modified mesenchymal stromal cells derived from adipose tissue". Cell Transplantation. 21 (9): 1997–2008. doi:10.3727/096368911X637452. PMID 22469297..
- [60]
^Zhao, Dawen; Richer, Edmond; Antich, Peter P.; Mason, Ralph P. (2008). "Antivascular effects of combretastatin A4 phosphate in breast cancer xenograft assessed using dynamic bioluminescence imaging and confirmed by MRI". The FASEB Journal. 22 (7): 2445–51. doi:10.1096/fj.07-103713. PMC 4426986. PMID 18263704..
- [61]
^Ow, D.W.; Wood, K.V.; DeLuca, M.; de Wet, J.R.; Helinski, D.R.; Howell, S.H. (1986). "Transient and stable expression of the firefly luciferase gene in plant cells and transgenic plants". Science. 234 (4778). American Association for the Advancement of Science. pp. 856–856. Bibcode:1986Sci...234..856O. doi:10.1126/science.234.4778.856. ISSN 0036-8075..
- [62]
^Altura, M.A.; Heath-Heckman, E.A.; Gillette, A.; Kremer, N.; Krachler, A.M.; Brennan, C.; Ruby, E.G.; Orth, K.; McFall-Ngai, M.J. (2013). "The first engagement of partners in the Euprymna scolopes-Vibrio fischeri symbiosis is a two-step process initiated by a few environmental symbiont cells". Environmental Microbiology. 15 (11): 2937–50. doi:10.1111/1462-2920.12179. PMC 3937295. PMID 23819708..
- [63]
^"Comprehensive Squid-Vibrio Publications List". University of Wisconsin-Madison. Archived from the original on 19 October 2014..
- [64]
^Ludwig Institute for Cancer Research (21 April 2003). "Firefly Light Helps Destroy Cancer Cells; Researchers Find That The Bioluminescence Effects Of Fireflies May Kill Cancer Cells From Within". Science Daily. Retrieved 4 December 2014..
- [65]
^"How illuminating". The Economist. 10 March 2011. Retrieved 6 December 2014..
- [66]
^(4 May 2013) One Per Cent: Grow your own living lights The New Scientist, Issue 2915, Retrieved 7 May 2013.
- [67]
^Dr. Chris Riley, "Glowing plants reveal touch sensitivity", BBC 17 May 2000..
- [68]
^Nic Halverson (August 15, 2013). "Bacteria-Powered Light Bulb Is Electricity-Free"..
- [69]
^Swaminathan, Miep. "Philips launches 'Microbial Home' new forward looking design concepts". Retrieved 8 May 2017.[永久失效连结].
- [70]
^Cha, Bonnie (28 November 2011). "Philips Bio-light creates mood lighting with bacteria"..
- [71]
^"E.glowli Cambridge: Parts submitted". iGEM. Retrieved 6 December 2014..
- [72]
^Marcellin, Frances (26 February 2016). "Glow-in-the-dark bacterial lights could illuminate shop windows 2016". New Scientist..
- [73]
^"Glowee: A vision of night-time lighting". EDF Pulse. Electricite de France. 2015. Retrieved 4 March 2016..
- [74]
^"Glow-in-the-dark bacterial lights could illuminate shop windows". New Scientist. 26 February 2016..
- [75]
^"Luminescence". Encyclopædia Britannica. Retrieved 16 December 2014..
暂无